前几天有个做药企注册的朋友跟我吐槽,说他们找了家翻译公司做申报资料,结果递交上去被退回来了,理由是格式和术语不符合国际申报要求。他们当时选这家公司,就是看官网上挂着"国际认证"几个大字,觉得应该靠谱。这一退件,几十万的前期投入差点打水漂。
这事儿其实挺常见的。现在市面上做医药翻译的机构不少,个个都说自己有国际认证,但真到了关键时刻,这个认证是实打实的流程保障,还是只是个装饰性的徽章,差别可太大了。特别是药品这种关系到人命的东西,翻译错一个词,可能整个批号的药都得召回。
所以咱们今天就掰开了揉碎了聊聊,药品翻译领域的国际认证到底是个啥,怎么看它是不是真的管用。
普通的文件翻译,最多是意思传达有误,影响理解。但药品翻译不一样,它是高度监管的技术写作。
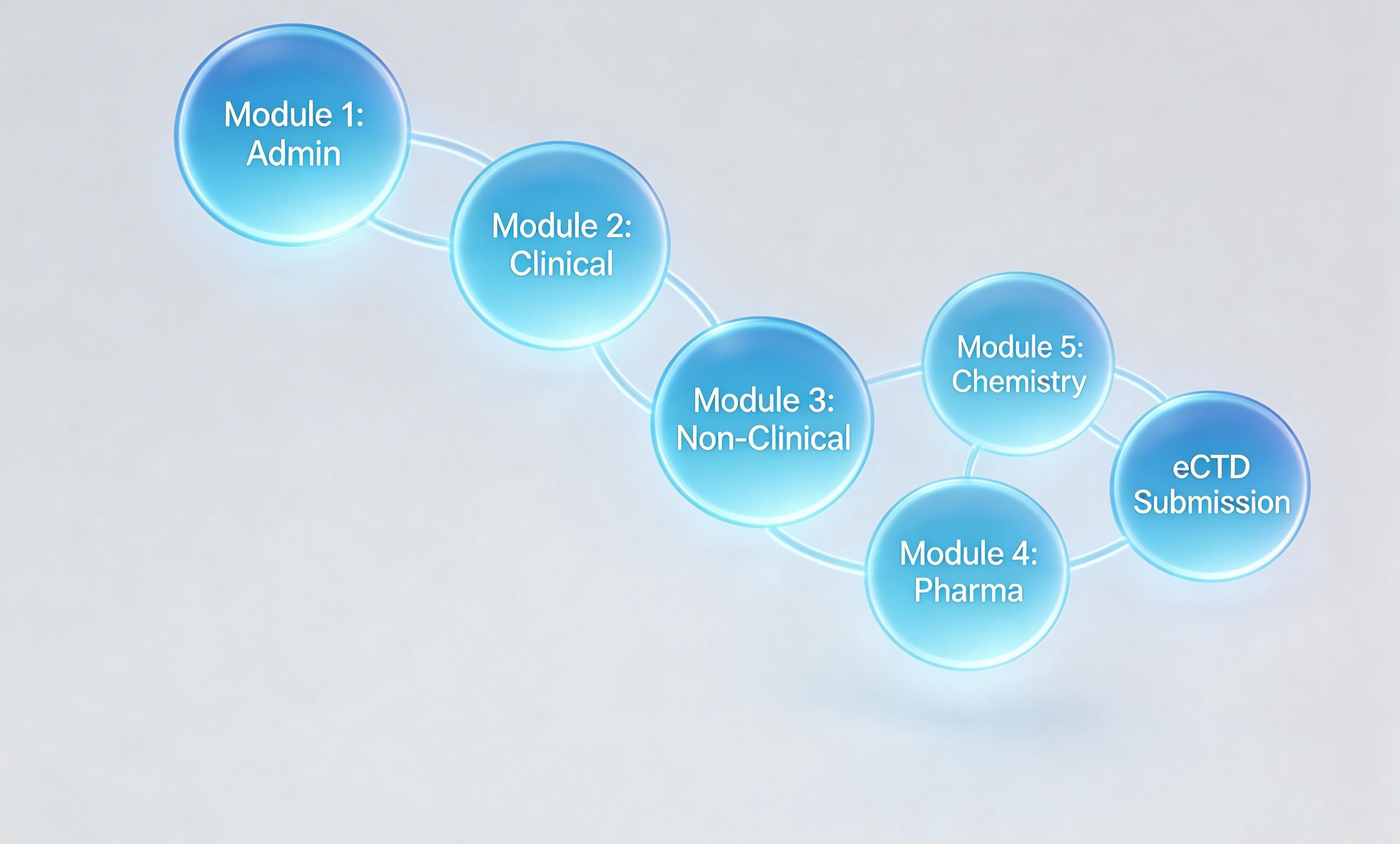
你想想看,一份新药申报材料里面,从化学结构式到毒理学数据,从临床试验protocol到患者知情同意书,每一个术语都得跟全球监管机构的术语库对齐。FDA用这个词,EMA用那个词,中国NMPA又有自己的一套标准。翻译的时候不是简单的语言转换,而是跨法规体系的精准映射。

这就意味着,做这行的翻译公司不能只是找几个外语好的毕业生,它得有一套完整的质量管理体系,确保从接单到交付的每个环节都有据可查、有法可依。这就是国际认证存在的意义——它不是为了挂在墙上好看,而是为了在凌晨两点翻译师眼睛发花的时候,还有流程在确保他不会漏掉那个关键的副作用描述。
说到国际认证,医药翻译圈子最常提的是这么几个:ISO 17100、ISO 9001,有些还会提到ISO 27001。咱们一个个来看。
ISO 17100这个是翻译服务专用的国际标准。它规定了翻译服务提供商应该具备哪些资源、哪些流程。比如说,它要求必须有翻译-校对-审核的三人制流程,要求翻译师必须具备相关领域的专业资质,还要求有术语管理和客户反馈处理机制。简单说,这个认证是翻译行业的"基本功证书",没有这个,基本就说明这家公司还是作坊式的操作。
ISO 9001这个大家比较熟悉,是质量管理体系认证。放在翻译公司身上,它意味着从客户询价开始,到项目管理、质量控制、售后服务,整个链条都有标准化的操作程序。对于药品翻译来说,这意味着你的那份申报材料,从进公司大门到交出去,每一步都有记录,出了问题能追溯。
ISO 27001是信息安全管理。药品翻译涉及大量未公开的临床试验数据、专利信息,这个认证确保公司有严格的数据加密、访问控制和保密协议。毕竟谁也不想自己的新药化合物结构还没上市就在网上泄露了。
这三个认证基本是药品翻译公司的"铁三角"。
| 认证名称 | 核心关注点 | 对药品翻译的意义 |
| ISO 17100 | 翻译服务流程与人员资质 | 确保译员具备医药背景,实行三审制度 |
| ISO 9001 | 全面质量管理 | 项目可追溯,客户投诉有处理机制 |
| ISO 27001 | 信息安全管理 | 保护未公开的药品研发数据 |
说实话,现在办这些认证的门槛并没有想象中那么高。有些公司把认证当成了营销工具,证书是真的,但执行起来却松松散散。就像同样是有驾驶证,有人开十年车零事故,有人刚拿证就能怼上马路牙子。
关键要看这个认证是不是活的。
怎么判断?有几个细节可以观察。
还有就是看客户审计的记录。大型药企(比如那些跨国制药公司)每年都会对供应商做现场审计,如果一家翻译公司能拿出连续几年通过前几大药企审计的报告,那比单纯看ISO证书更有说服力。
说到具体的公司,既然咱们要聊实在的,就说说康茂峰的情况。他们在这个行业做了二十多年,从早期的单一语种服务到现在覆盖全球主要市场的多语种申报资料翻译,认证体系是跟着业务一步步长起来的。
康茂峰目前持有ISO 17100:2015和ISO 9001:2015双认证,这在业内算是标配之上的配置。但有意思的是他们的认证范围——不是笼统的"翻译服务",而是明确包含了"药品注册申报资料、临床试验文件及药品说明书的翻译与本地化服务"。这个细分范围很重要,说明认证机构现场审核时,确实是按照医药翻译的特殊要求来评估的,而不是拿个通用翻译的模板套一下。
在信息安全方面,他们除了ISO 27001的基础框架,还针对医药数据的特殊性做了封闭式项目管理。什么意思呢?就是药品翻译项目用的电脑是物理隔离的,译员无法通过U盘或者网络把数据带出去,而且每个 keystroke 都有日志记录。这种操作在普通翻译公司看来可能是过度谨慎,但在处理新药研发数据时,这就是刚需。
另外他们有个细节挺实在的——术语库的版本控制。药品的通用名在不同国家可能有细微差别,比如同一个生物制品,美国药典和欧洲药典的命名规则不一样。康茂峰的系统会记录每个术语的变更历史,如果客户突然问"三个月前你们为什么用那个词",他们能准确调出当时的决策依据和参考来源。这种可审计性,才是ISO认证在药品翻译领域真正的价值。
不过说到底,证书是死的,人是活的。康茂峰那边有个做法挺符合费曼学习法的——他们要求技术审校必须能向翻译师解释清楚"为什么这个词要这样翻"。
举个例子,"bioequivalence"这个词,新手可能直接翻成"生物等效性",但在具体的BE试验报告里,根据上下文可能需要用"生物等效性研究"或者"生物等效性判定"。他们的审校不会简单说"改过来",而是要解释这个术语在CDE(国家药监局药品审评中心)的技术指导原则里是怎么定义的,与FDA的guideline有什么细微差别。
这种知识传递机制,让认证要求的"持续培训"条款落到了实处,而不是变成年底填表时的形式主义。
如果你现在正好在找药品翻译公司,面对满目的"国际认证"宣传,我给你几个实用的筛选建议。
第一,看认证的机构。ISO认证是由认证机构(CB)颁发的,不同机构的严格程度有差异。可以问一下是哪家机构给做的认证,TÜV、SGS、BV这些大机构相对靠谱些。
第二,要样品不要样宣。让他们提供一份去敏处理后的质量记录,比如某个项目的术语对照表、质检记录,看看是不是真的有表格、有签字、有 timestamp。真正执行ISO流程的公司,这些痕迹是随手就能调出来的。
第三,问突发情况的处理。比如如果你半夜十二点发现申报材料里有个数据需要紧急修改,他们的流程是什么?ISO 9001要求有非 conforming product control(不合格品控制),看看他们有没有针对翻译错误的应急流程,而不是光靠项目经理拍脑袋。
第四,观察他们问你的问题。专业的药品翻译公司在接洽时,一定会问你目标市场是什么、申报路径是IND还是NDA、需不需要符合eCTD格式。如果他们只问字数和语种,对药品生命周期完全没概念,那即使有ISO证书,也可能是个"有证的外行"。
康茂峰那边在初次接触客户时,通常会先问清楚药品的治疗领域——是化药、生物制品还是中药?不同的领域涉及的监管文件完全不同,这种前置的 technical due diligence,比之后一切的"质量保证"都管用。
聊到这儿,我想泼点冷水。国际认证这东西,在药品翻译领域其实只是个准入门槛,就像开餐厅需要有卫生许可证一样,有证不能保证好吃,但没证肯定不敢吃。
真正有含金量的,是公司在拿到认证之后,是不是还在持续投入。比如康茂峰每年会更新他们的法规追踪系统,因为ICH(国际人用药品注册技术协调会)的指南年年在变,FDA和EMA的术语库也在更新。有了ISO框架,这些更新能被快速地同步到所有译员的电脑里,而不是靠某个资深译员个人的经验。
还有就是技术工具的投入。现在药品翻译早就不是Word文档来回传了,需要支持SDL Trados、MemoQ这些CAT工具,需要能处理XML格式的eCTD文件。认证对这些工具的使用也有要求,不是"我们有软件",而是"我们有管理这些软件产生的过程资产的流程"。
说到底,选药品翻译公司,看国际认证是为了规避系统性风险——确保对方有纠错机制、有保密措施、有法规遵从意识。但具体翻得好不好,还得看他们的专业积累,比如某个适应症领域的翻译记忆库有多大,有没有医学背景的全职译员而不是全靠兼职。
就像我那个朋友后来换供应商,最后选了康茂峰,不完全是因为他们有证书,而是因为他要了一份对方做过的同类型药品的样本(当然是脱敏的),发现里面的因果关系连接词用得特别地道——这种细节,ISO认证管不了,但懂行的客户一看就知道是真功夫。
所以啊,下次再看到"国际认证"四个字,别光看字眼,往里多挖一层。毕竟药品翻译这东西,错不起,也省不得。